
A Peptidalapú Vakcinák Kutatócsoport 2021-ben alakult az MTA Lendület Programjának támogatásával. A csoportban előállított peptideket, peptid-származékokat és konjugátumokat különböző kutatási területeken alkalmazzuk. A szintetikus peptidek biológiai hatásának fokozására és stabilitásuk megőrzésére új formulációs stratégiákat dolgozunk ki. Kolloidkémiai rendszerek segítségével peptidhordozó platformokat fejlesztünk, melyek számos előnyös tulajdonsággal rendelkeznek, mint a célbajuttatás, programozott hatóanyag-leadás és fokozott immunogenitás.
Fő kutatási témák
– Szintetikus vakcinák
– Dendritikus sejtek célzása peptidekkel
– Antimikrobiális peptidek és peptid-származékok
– Szintetikus vakcinák az immunterápiában
– Melanoma specifikus peptidek és peptid-származékok
A Biological Soft Matter Platform honlapja
Tagok
Horváti Kata, kutatócsoport-vezető
Szabó Ildikó, tudományos főmunkatárs
Gyulai Gergő, tudományos munkatárs
Kiss Krisztina, tudományos munkatárs
Kőműves Tamás, PhD hallgató
Gellény Szabolcs, hallgató
Pintér Bence, hallgató
Kóczán Katalin, kutatói asszisztens
Hírek
New year, new positions!
 We are offering 15 positions for early-stage researchers to participate in the EVADERE (Enhanced VAccines DEsign against antimicrobial REsistance) program, an EU-funded Marie Skłodowska-Curie PhD training network, in the fields of medicinal chemistry, immunology, microbiology, medical sciences, and vaccinology. If you want to make a difference in the global fight against antimicrobial resistance, sign up for the program! The information and requirements for applying can be found here: https://evadere1.eu/jobs.
We are offering 15 positions for early-stage researchers to participate in the EVADERE (Enhanced VAccines DEsign against antimicrobial REsistance) program, an EU-funded Marie Skłodowska-Curie PhD training network, in the fields of medicinal chemistry, immunology, microbiology, medical sciences, and vaccinology. If you want to make a difference in the global fight against antimicrobial resistance, sign up for the program! The information and requirements for applying can be found here: https://evadere1.eu/jobs.At the HUN-REN TTK AKI the doctoral candidate (DC) will be trained in peptide synthesis and related organic chemistry to produce multi-epitope vaccine constructs. In cooperation with our industrial partner, Cyclolab, we will provide training in vaccine delivery and formulation techniques, as well as related analytical and characterization methods. In the host group, DC will receive training in working with cell cultures and performing basic biological studies (cell viability tests, cellular uptake, and cytokine production assays), and will work, in collaboration with other DCs, on adjuvant delivery, microneedle patches and vaccine efficacy tests.
Deadline: April 30, 2026, 5:00 p.m. GMT. Start of the PhD program: September 1, 2026.
Chemical Singers karácsonyi koncert

Idén is csodás hangulatban telt a Chemical Singers kórus karácsonyi koncertje, melyhez pár éve csatlakozott kutatócsoportunk
Kutatócsoportunk csatlakozott a SNOOPY – COST ACTION CA23111 programhoz

Kutatócsoportunk csatlakozott a SNOOPY – COST ACTION CA23111 programhoz. A SNOOPY (Searching for Nanostructured or pOre fOrming Peptides for therapY) különböző tudományágak (kémia, biológia, biokémia, anyagtudomány, nanotechnológia, orvostudomány, fizika) fiatal kutatóiból álló hálózat, melynek célja a bioaktív peptidek funkcionális nanostruktúrákba való önszerveződésének feltérképezése. A program 4 munkacsomagot foglal magában, melyek közül a WG2 csapathoz csatlakoztunk. A WG2 peptidek és nanostruktúrák előállításával, fenntarthatóságának és hatékonyságának javításával foglalkozik. Első konferenciánk 2026 januárjában lesz Notthingham-ben, ahol Horváti Kata a lipopeptidek önszerveződéséről és formulációjáról fog előadást tartani. https://cost-snoopy.eu/news/first-snoopy-wg2-meeting/
STEM Talk beszélgetés a Nobel-díjas Karikó Katalinnal Berlinben, Horváti Kata (HUN-REN TTK) részvételével
Egy fantasz tikusan inspiráló előadás után, a Nobel-díjas Karikó Katalinnal beszélgethettünk 2025. november 10-én a berlini magyar nagykövetségen, ahol a Berlini Tudományos Hét keretében egy STEM Talk esemény került megrendezésre német és magyar fiatal kutatók részvételével.
tikusan inspiráló előadás után, a Nobel-díjas Karikó Katalinnal beszélgethettünk 2025. november 10-én a berlini magyar nagykövetségen, ahol a Berlini Tudományos Hét keretében egy STEM Talk esemény került megrendezésre német és magyar fiatal kutatók részvételével.
A német Die Junge Akademie képviseletében az igazgatótanács tagja, Hani Harb immunológus jelent meg, aki a Drezdai Műszaki Egyetem adjunktusa. A Fiatal Kutatók Akadémiáját Horváti Kata képviselte, aki az MTA–HUN-REN TTK Lendület Peptidalapú Vakcinák Kutatócsoport vezetője. A rendezvény moderálását Victoria Azarov, a Semmelweis Egyetem orvostanhallgatója és a STEMtalk podcast sorozat alkotója végezte.
A főprogram előtt a Szegedi Tudományegyetem küldöttsége mutatta be a „Forever Forward – Katalin Karikó” című kiállítást, mely a Nobel-díjas kutató életpályájának legfontosabb momentumait és díjait sorakoztatja fel.

A délután Dr. Györkös Péter, Magyarország nagykövetének üdvözlő beszédével kezdődött, majd Karikó Katalin „A Karikó-módszer” című előadása következett, amelyben megosztotta velünk életének történetét, annak minden nehézségével együtt, és erőteljes üzeneteket közvetített a kutató bátorságról, rugalmasságról és – Selye Jánost idézve – a stresszről és annak kezeléséről.
Az előadás után panelbeszélgetés következett a kutatói karrierútvonalakról, a mobilitásról, publikációs stratégiákról, a fiatal kutatókat érintő kihívásokról és a tudományos kitartásról.
A közönség kíváncsi és merész kérdéseket tett fel, melyet Karikó Katalin a maga szellemes és végtelenül intelligens módján válaszolt meg, majd a beszélgetés egy fogadáson folytatódhatott. A hangulat nagyon inspiráló volt és erőteljes, tele tudománnyal és jókedvvel.
A Magyar Mikrobiológiai Társaság által szervezett nemzetközi konferencián vett részt a csoportunk

A 2025. október 6-8. között Siófokon megrendezett konferencián Kiss Krisztina, Kőműves Tamás és Horváti Kata képviselte a kutatócsoportot. A CEFORM 7th Central European Forum for Microbiology rendezvényen bemutatott poszter peptidalapú hatóanyagok számára készített poloxamer micellákról szólt.

Kezdődhet az EVADERE projekt!
Az EVADERE (Enhanced VAccines DEsign against antimicrobial REsistance) projektünk 97,5%-os pontszámmal támogatást nyert az MSCA-DN program keretében. A Marie Skłodowska Curie Doktori Hálózatok pályázati konstrukció a Horizont Európa keretében, doktori hallgatók bevonásával és képzésével megvalósított közös kutatási projekteket támogat. Az EVADERE projekt várhatóan 2026 nyarán indul és fő célkitűzése az antimikrobiális rezisztencia ellen új antigének, adjuvánsok és hordozórendszerek fejlesztése. A HUN-REN TTK Peptid-alapú Vakcinák Kutatócsoportja munkacsomag-vezetőként vesz részt a pályázatban. A multidiszciplináris konzorciumban 8 európai országból 11 egyetemi és 2 ipari kutatócsoport vesz részt, és a PhD pozíciók az EURAXESS portálon fognak megjelenni.
Köszönet mindenkinek, aki hozzájárult ehhez a sikerhez!

Kőműves Tamás tudományos diákköri sikerei
Kőműves Tamás a Semmelweis Egyetem idei Tudományos Diákköri Konferenciáján, Gyógyszertudományok (B) szekcióban 1. helyezést ért el, így részt vehetett a 37. Országos Tudományos Diákköri Konferencián, ahol az Orvos- és Egészségtudományi Szekcióban a zsűri külön díjában részesült. Témavezetője Horváti Kata, dolgozatának címe: Kationos lipopeptidek szintézise és azok antimikrobiális hatásának vizsgálata.
Eredményéhez szívből gratulálunk!


Chiara Bellini sikeresen megvédte doktori disszertációját
2024. november 14-én diákunk, Chiara Bellini sikeresen megvédte doktori disszertációját, summa cum laude minősítéssel. Chiara, Horváti Kata témavezetésével, peptidalapú vakcinákat fejlesztett a tuberkulózis ellen. Doktori munkáját az EU H2020-MSCA-ITN program keretében végezte, a BactiVax (https://cordis.europa.eu/project/id/860325) projekt résztvevőjeként. Képzése során lehetősége nyílt a CycloLab Kft-ben (https://cyclolab.hu/) is kutatásokat végezni, Puskás István irányításával.
Publikációk
2025
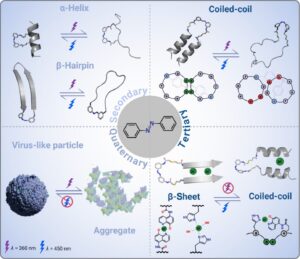 E Erdei, J T Marcos, N Varró, K Horváti, B Bacsa, I M. Mándity: Spatiotemporal control in biomedicine: photoswitchable peptides and foldamers. Br J Pharmacol. 2025;1–8. https://doi.org/10.1111/bph.70163. [IF(2024):7.7] D1
E Erdei, J T Marcos, N Varró, K Horváti, B Bacsa, I M. Mándity: Spatiotemporal control in biomedicine: photoswitchable peptides and foldamers. Br J Pharmacol. 2025;1–8. https://doi.org/10.1111/bph.70163. [IF(2024):7.7] D1
Chakraborty S., el Battioui K., Sonallya T., Szigyártó I.C., Horváti K., Varga Z., Juhász T., Beke-Somfai T.: Charge and length dependent build-up of environment sensitive lamellin β-peptides (2025) Physical Chemistry Chemical Physics, 27 (16), pp. 8540 – 8551. https://doi.org/10.1039/D4CP04561K [IF(2024):2.9] Q1
Fecske, D.; Kasza, Gy.; Gyulai, G.; Horváti, K.; Szabó, M.; Wacha, A.; Varga, Z.; Szarka, Gy.; Thomann, Y.; Thomann, R.; Mülhaupt, R.; Kiss, É.; Domján, A.; Bősze, Sz.; Bereczki, L.; Iván, B.
Self-Assembling Amphiphilic ABA Triblock Copolymers of Hyperbranched Polyglycerol with Poly(tetrahydrofuran) and Their Nanomicelles as Highly Efficient Solubilization and Delivery Systems of Curcumin. Int. J. Mol. Sci. (2025), 26, 5866. https://doi.org/10.3390/ijms26125866 [IF(2023):4.9]
Chiara Bellini, Unai Atxabal, Szilvia Bősze, Orsolya Dobay, Andrea Horváth, Imola Cs. Szigyártó, Tamás Beke-Somfai, Jesús Jiménez-Barbero, István Puskás, Kata Horváti*: Supramolecular complexes of ultrashort cationic lipopeptides with cyclodextrins: improved selectivity and therapeutic potential. Aggregate (2025) 0:e741; https://doi.org/10.1002/agt2.741 [IF(2023):13.9] D1
2024
 Ágnes Ábrahám, Gergő Gyulai, Judith Mihály, Andrea Horváth, Orsolya Dobay, Zoltán Varga, Éva Kiss, Kata Horváti*: Optimizing lipopeptide bioactivity: The impact of non-ionic surfactant dressing, J Pharm Anal. (2024) 101020, https://doi.org/10.1016/j.jpha.2024.101020 [IF:8.9] D1
Ágnes Ábrahám, Gergő Gyulai, Judith Mihály, Andrea Horváth, Orsolya Dobay, Zoltán Varga, Éva Kiss, Kata Horváti*: Optimizing lipopeptide bioactivity: The impact of non-ionic surfactant dressing, J Pharm Anal. (2024) 101020, https://doi.org/10.1016/j.jpha.2024.101020 [IF:8.9] D1
El Battioui K, Chakraborty S, Wacha A, Molnár D, Quemé-Peña M, Szigyártó IC, Szabó CL, Bodor A, Horváti K, … Beke-Somfai T. In situ captured antibacterial action of membrane-incising peptide lamellae. Nat Commun. (2024) 15(1):3424. doi: 10.1038/s41467-024-47708-4. [IF(2023):14.7] D1
György Kasza, Ákos Fábián, Dóra Fecske, Attila Kardos, Róbert Mészáros, Kata Horváti, Béla Iván. Hyperbranched polyglycerol grafted poly(N,N-diethylacrylamide) thermoresponsive copolymers as biocompatible, highly efficient encapsulation and sustained release systems of curcumin. Eur Polymer J (2024) 219:113378. https://doi.org/10.1016/j.eurpolymj.2024.113378 [IF:6.3] Q1
Humer C, Radiskovic T, Horváti K, Lindinger S, Groschner K, Romanin C, Höglinger C: Bidirectional allosteric coupling between PIP2 binding and the pore of the oncochannel TRPV6. Int. J. Mol. Sci. (2024), 25(1), 618; https://doi.org/10.3390/ijms25010618 [IF:4.9] Q1
2023
 Bellini C, Vergara E, Bencs F, Fodor K, Bősze S, Krivić D, Bacsa B, Surguta SE, Tóvári J, Reljic R, Horváti K*. Design and characterization of a multistage peptide-based vaccine platform to target Mycobacterium tuberculosis infection. Bioconjug Chem. (2023) 34:1738-1753. https://doi.org/10.1021/acs.bioconjchem.3c00273 [IF:6.069] D1
Bellini C, Vergara E, Bencs F, Fodor K, Bősze S, Krivić D, Bacsa B, Surguta SE, Tóvári J, Reljic R, Horváti K*. Design and characterization of a multistage peptide-based vaccine platform to target Mycobacterium tuberculosis infection. Bioconjug Chem. (2023) 34:1738-1753. https://doi.org/10.1021/acs.bioconjchem.3c00273 [IF:6.069] D1
Tóth G, Horváti K, Kraszni M, Ausbüttel T, Pályi B, Kis Z, Mucsi Z, Kovács G M, Bősze Sz, Boldizsár I. Arylnaphthalene lignans with anti-SARS-CoV-2 and antiproliferative activities from the underground organs of Linum austriacum and Linum perenne. J Nat Prod (2023) 86(4): 672–682. https://doi.org/10.1021/acs.jnatprod.2c00580 [IF:4.803] Q1
2021
Horváti K, Fodor K, Pályi B, Henczkó J, Balka Gy, Gyulai G, Kiss É, Biri-Kovács B, Senoner Zs, Bősze Sz. Novel assay platform to evaluate intracellular killing of Mycobacterium tuberculosis: in vitro and in vivo validation. Front Immunol. (2021) 12:750496. doi: 10.3389/fimmu.2021.750496 [IF: 8.786] Q1
Juhász T, Quemé-Peña M, Kővágó B, Mihály J, Ricci M, Horváti K, Bősze S, Zsila F, Beke-Somfai T. Interplay between membrane active host defense peptides and heme modulates their assemblies and in vitro activity. Sci Rep. (2021) 11(1):18328. https://www.nature.com/articles/s41598-021-97779-2 [IF: 4.996] Q1
Farkas V, Ferentzi K, Horváti K, Perczel A. Cost-Effective Flow Peptide Synthesis: Metamorphosis of HPLC. Org. Process Res. Dev. (2021) 25(2) 182–191. https://doi.org/10.1021/acs.oprd.0c00178 [IF: 3.858] (independent citations: 1)
Zürn M, Tóth G, Ausbüttel T, Mucsi Z, Horváti K, Bősze Sz, Sütöri-Diószegi M, Pályi B, Kis Z, Noszál B, Boldizsár I. (2021) Tissue specific accumulation and isomerization of valuable phenylethanoid glycosides from Plantago and Forsythia plants. Int. J. Mol. Sci. 2021, 22(8), 3880. https://doi.org/10.3390/ijms22083880 [IF(2010): 5.924] Q1
Kósa N, Zolcsák Á, Voszka I, Csík G, Horváti K, Horváth L, Bősze Sz, Herenyi L. (2021) Comparison of the efficacy of two novel antitubercular agents in free and liposome-encapsulated formulations. Int. J. Mol. Sci. 2021, 22(5), 2457. https://doi.org/10.3390/ijms22052457 [IF: 6.208] Q1
Quemé-Peña M, Ricci M, Juhász T, Horváti K, Bősze S, Biri-Kovács B, Szereder B, Zsila F, Beke-Somfai T. (2021) Old Polyanionic Drug Suramin Suppresses Detrimental Cytotoxicity of the Host Defense Peptide LL-37. ACS Pharmacol. Transl. Sci. 4(1) 155–167. https://doi.org/10.1021/acsptsci.0c00155
2020
Bellini C, Horváti K*. Recent advances in the development of protein- and peptide-based subunit vaccines against tuberculosis. Cells 2020, 9(12), 2673; https://doi.org/10.3390/cells9122673. [IF: 6.600]
Pári E, Horváti K, Bősze S, Biri-Kovács B, Szeder B, Zsila F, Kiss É. Drug Conjugation Induced Modulation of Structural and Membrane Interaction Features of Cationic Cell-Permeable Peptides. Int J Mol Sci. 2020 21(6). pii: E2197. doi: 10.3390/ijms21062197. [IF: 5.924]
Ricci M, Horváti K, Juhász T, Szigyártó I, Török Gy, Sebák F, Bodor A, Homolya L, Henczkó J, Pályi B, Mlinkó T, Mihály J, Nizami1 B, Yang Z, Lin F, Lu X, Románszki L, Bóta A, Varga Z, Bősze Sz, Zsila F, Beke-Somfai T. (2020) Anionic food color Tartrazine enhances antibacterial efficacy of Histatin-derived peptide DHVAR4 by fine-tuning its membrane activity. Quarterly Rev Biophysics 53, e5, 1–11. https://doi.org/10.1017/S0033583520000013 [IF:5.318]
2019
Horváti K*, Pályi B, Henczkó J, Balka Gy, Szabó E, Farkas V, Biri-Kovács B, Szeder B, Fodor K. (2019) A convenient synthetic method to improve immunogenicity of Mycobacterium tuberculosis related T-cell epitope peptides. Vaccines 7(3), 101. https://doi.org/10.3390/vaccines7030101 [IF:4.086]
Zürn M, Tóth G, Mazákné Kraszni M, Sólyomváry A, Mucsi Z, Deme R, Rózsa B, Fodor B, Molnár-Perl I, Horváti K, Bősze Sz, Pályi B, Kis Z, Béni Sz, Noszál B, Boldizsár I. (2019) Galls of European Fraxinus trees as new and abundant sources of valuable phenylethanoid and coumarin glycosides. Industrial Crops and Products 139: 111517-26. https://doi.org/10.1016/j.indcrop.2019.111517 [IF: 4.244]
Gyulai G., Ouanzi F., Bertóti I., Mohai M., Kolonits T., Horváti K., Bősze S. Chemical structure and in vitro cellular uptake of luminescent carbon quantum dots prepared by solvothermal and microwave assisted techniques. J. Colloid Interface Sci. 2019, 549, 150-161. https://doi.org/10.1016/j.jcis.2019.04.058 [IF: 7.361]
Quemé-Peña M, Juhász T, Mihály J, Szigyártó IC, Horváti K, Bősze S, Henczkó J, Pályi B, Németh C, Varga Z, Zsila F, Beke-Somfai T. (2019) Manipulating active structure and function of cationic antimicrobial peptide CM15 by the polysulfonated drug suramin: a step closer to in vivo complexity. ChemBioChem 20:1–14. https://doi.org/10.1002/cbic.201800801 [IF: 2.576]
2018
Ábrányi-Balogh P, Petri L, Imre T, Szijj P, Scarpino A, Hrast M, Mitrovic A, Fonovic UP, Németh K, Barreteau H, Roper DI, Horváti K, Ferenczy GyG, Kos J, Ilas J, Gobec S, Keserű GyM. (2018) A road map for prioritizing warheads for cysteine targeting covalent inhibitors. Eur J Med Chem. 2018. 160:94-107. https://doi.org/10.1016/j.ejmech.2018.10.010 [IF: 4.816]
Kiss É, Gyulai G, Pári E, Horváti K, Bősze S. (2018) Membrane affinity and fluorescent labelling: comparative study of monolayer interaction, cellular uptake and cytotoxicity profile of carboxyfluorescein-conjugated cationic peptides. Amino Acids 50(11):1557-1571. doi: 10.1007/s00726-018-2630-7 [IF: 2.906]
Horváti K, Gyulai G, Csámpai A, Rohonczy J, Kiss É, Bősze Sz (2018) Surface layer modification of PLGA nanoparticles with targeting peptide: a convenient synthetic route for Pluronic F127 – Tuftsin conjugate. Bioconjugate Chem. 29(5):1495-1499. https://doi.org/10.1021/acs.bioconjchem.8b00156 [IF: 4.818]
Zsila F, Juhász T, Bősze Sz, Horváti K, Beke-Somfai T (2018) Hemin and bile pigments are the secondary structure regulators of intrinsically disordered antimicrobial peptides. Chirality 30(2):195-205. https://doi.org/10.1002/chir.22784 [IF: 1.956]
Sipka S, Papp Zs, Kovács I, Horváti K, Bősze Sz, Hudecz F, Szilasi M (2018) Index of stimulation and TNFα measurements used for laboratory diagnosis of latent Tuberculosis as a new principle. Int J Pulmonol Infect Dis.1(2):1-5. DOI:10.15226/2637-6121/1/2/00108
2017
Horváti K, Bacsa B, Mlinkó T, Szabó N, Hudecz F, Zsila F, Bősze Sz (2017) Comparative analysis of internalisation, haemolytic, cytotoxic and antibacterial effect of membrane-active cationic peptides: aspects of experimental setup. Amino Acids. 49(6):1053-1067. DOI: 10.1007/s00726-017-2402-9 [IF: 2.906]
Zsila F, Bősze Sz, Horváti K, Szigyártó CsI, Beke-Somfai T (2017) Drug and dye binding induced folding of the intrinsically disordered antimicrobial peptide CM15. RSC Advances 7:41091-41097. DOI: 10.1039/c7ra05290a [IF: 2.936]
2016
Ábrahám Á, Baranyai Zs, Gyulai G, Pári E, Horváti K, Bősze Sz, Kiss É (2016) Comparative analysis of new peptide conjugates of antitubercular drug candidates-model membrane and in vitro studies. Colloids Surf B Biointerfaces. 28(147):106-115. https://doi.org/10.1016/j.colsurfb.2016.07.054 [IF: 3.887]
Horvati K, Bősze Sz, Gideon HP, Bacsa B, Szabó TG, Goliath R, Rangaka MX, Hudecz F, Wilkinson RJ, Wilkinson KA (2016) Population tailored modification of tuberculosis specific interferon-gamma release assay. J Infection 72:179-188. https://doi.org/10.1016/j.jinf.2015.10.012 [IF: 4.201]
2015
Horváti K, Bacsa B, Szabó N, Fodor K, Balka G, Rusvai M, Kiss É, Mező G, Grolmusz V, Vértessy B, Hudecz F, Bősze Sz (2015) Antimycobacterial activity of peptide conjugate of pyridopyrimidine derivative against Mycobacterium tuberculosis in a series of in vitro and in vivo models. Tuberculosis: 95:S207-211. https://doi.org/10.1016/j.tube.2015.02.026 [IF: 2.952]
Baranyai Zs, Krátký M, Vinšová J, N Szabó N, Senoner Zs, Horváti K, Stolaříková J, Dávid S, Bősze Sz (2015) Combating highly resistant emerging pathogen Mycobacterium abscessus and Mycobacterium tuberculosis with novel salicylanilide esters and carbamates, Eur J Med Chem 101:692-704. https://doi.org/10.1016/j.ejmech.2015.07.001 [IF: 3.902]
2014
Horváti K, Bacsa B, Kiss E, Gyulai G, Fodor K, Balka G, Rusvai M, Szabó E, Hudecz F, Bősze Sz (2014) Nanoparticle encapsulated lipopeptide conjugate of antitubercular drug isoniazid: in vitro intracellular activity and in vivo efficacy in a Guinea pig model of tuberculosis. Bioconjug Chem. 25(12):2260-2268. https://doi.org/10.1021/bc500476x [IF: 4.513]
Kiss É, Gyulai G, Pénzes CB, Idei M, Horváti K, Bacsa B, Bősze Sz (2014) Tunable surface modification of PLGA nanoparticles carrying new antitubercular drug candidate. Colloid Surface A. 458: 178-186. https://doi.org/10.1016/j.colsurfa.2014.05.048 [IF: 2.752]
Cserép GB, Baranyai Z, Komáromy D, Horváti K, Bősze Sz, Kele P (2014) Fluorogenic tagging of peptides via Cys residues using thiol-specific vinyl sulfone affinity tags. Tetrahedron 70(35): 5961-5965. https://doi.org/10.1016/j.tet.2014.05.103 [IF: 2.641]
2013
Misják P, Bősze Sz, Horváti K, Pasztói M, Palóczi K, Holub MC, Szakács F, Aradi B, György B, Szabó TG, Nagy G, Glant TT, Mikecz K, Falus A, Buzás EI (2013) The role of citrullination of an immunodominant proteoglycan (PG) aggrecan T cell epitope in BALB/c mice with PG-induced arthritis. Immunol Lett. 152: 25-31. https://doi.org/10.1016/j.imlet.2013.03.005 [IF: 2.367]
2012
Horváti K, Bacsa B, Szabó N, Dávid S, Mező G, Grolmusz V, Vértessy B, Hudecz F, Bősze Sz (2012) Enhanced cellular uptake of a new, in silico identified antitubercular candidate by peptide conjugation. Bioconjug Chem. 23: 900-907. https://doi.org/10.1021/bc200221t [IF: 4.580]
Pénzes CB, Schnoller D, Horváti K, Bősze Sz, Mező G, Kiss É (2012) Membrane affinity of antituberculotic drug conjugate using lipid monolayer containing mycolic acid. Colloid Surfaces A. 413: 142-148. https://doi.org/10.1016/j.colsurfa.2012.02.013 [IF: 2.108]
Munkatársak


