Kutatási terület
- Bioortogonális reagensek fejlesztése, bioortogonalizált fluoreszcens jelzővegyületek szintézise, bioortogonalizált fluorogén vegyületek szintézise, fehérjék genetikai manipulációja, upconverting nanorészecske alapú gyógyszerhatóanyag-hordozók szintézise, photo-crosslinker módosított ligandumok szintézise
- az asztrociták neuronális aktivitást befolyásoló szerepének vizsgálata egészséges és beteg agyban
- potenciálisan gyógyszerfejlesztésre alkalmas (elsősorban asztrogliális) célfehérjék és -mechanizmusok azonosítása patofiziológiás körülmények között
- toxikológiai teszt platformok fejlesztése és alkalmazása gyógyszerfejlesztési projektekhez
A fenti kutatási területek vizsgálatára multidiszciplináris, in vitro és in vivo fluoreszcens képalkotási, elektrofiziológiai, toxikológiai módszereket, valamint szerves szintetikus megközelítéseket alkalmazunk.
Kutatási témák
Az asztrociták hozzájárulása a neuronális szinkronizációkhoz egészséges és kóros állapotokban
Az asztrocitáknak hosszú időn át kizárólag metabolikus támogató szerepet tulajdonítottak a központi idegrendszerben. Az utóbbi két évtized felfedezései azonban az idegrendszeri ingerületátvitel fontos szereplőiként azonosították őket, akik jelentős szerepet játszanak a neuronális aktivitás szabályozásában mind fiziológiás, mind patofiziológiás körülmények között (Héja, 2014). Korábbi munkáinkban elektrofiziológiai és képalkotó módszerekkel vizsgáltuk, hogy az asztrogliális aktivitást jól reprezentáló Ca2+ ion tranziensek megjelenése megfelel-e a neuronális aktivitás térbeli mintázatának. Kimutattuk, hogy a neuronális epileptiform kisülésekhez kapcsolódóan az asztrociták is szinkronizált aktivitást produkálnak, mely asztrogliális roham-szerű eseményekké evolválódik (Kékesi et al., 2015). Vagyis az asztrocitáknak megvan az a képessége, hogy indukálják a kóros mértékű neuronális szinkronizáció kialakulását epilepsziában.
A fenti kutatások kiterjesztéseként vizsgáljuk továbbá, hogy az asztrociták hozzájárulnak-e egyes fiziológiás neuronális szinkronizációk, mint például a memória konszolidációban kulcsszerepet játszó alvási lassú hullám aktivitások kialakulásához. Ennek céljából egy, a kutatóközpont Biomembrán Kutatócsoportjával (EI) kooperációban létrehozott új, Ca2+ ion szenzor fehérjét kifejező transzgenikus patkányokat használunk. Ezen állatokat sikeresen használtuk a neuronális és asztrogliális aktivitás alvás alatti párhuzamos monitorozására in vivo. Kimutattuk, hogy az asztrocita hálózat szinkronizációja megelőzi a neuronális szinkronizáció kialakulását, ami arra utal, hogy az asztrocita syncytiumnak oksági szerepe van a lassú-hullám aktivitás létrehozásában.
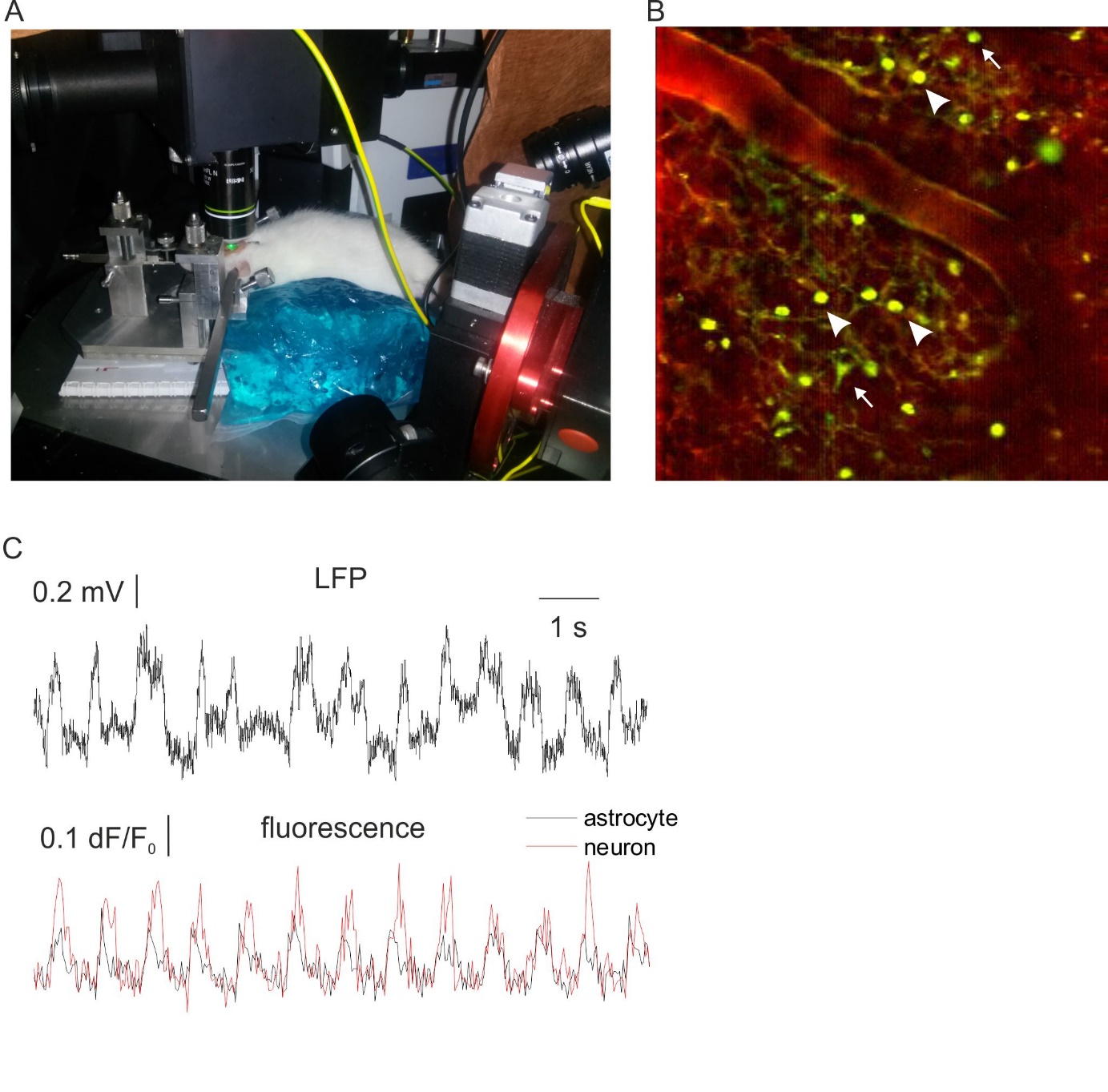 |
| Mind az asztrociták, mind a neuronok aktívak az in vivo lassú-hullám aktivitás alatt. A: A GCaMP2 fehérjét expresszáló stabil transzgenikus patkány vonal in vivo vizsgálata. B: A GCaMP2 fehérje (zöld) kifejeződése és az asztrociták megjelölése intravénásan alkalmazott SR101 festékkel (piros). Mind a neuronok (nyilak), mind az asztrociták (nyílhegyek) kifejezik a GCaMP2 fehérjét. C: A lokális mezőpotenciál (LFP) és a neuronális (fekete) és asztrogliális (piros) Ca2+ ion tranziensek egyidejű detektálása lassú-hullám aktivitás alatt. |
Astrogliális neurotranszmitter transzporterek és réskapcsolat fehérjék, mint potenciális anti-epileptikumok
Korábban kimutattuk, hogy az asztrociták jelentősen hozzájárulnak a neuronokra ható tónusos gátlás kialakításához azáltal, hogy GABA-t szabadítanak fel. A gliális Glu/GABA cserefolyamatot (Héja et al., 2009, 2012) a szinaptikusan felszabaduló Glu gliális felvétele váltja ki. A létrejövő asztrogliális negatív visszacsatolás mértéke arányos a hálózati aktivitás nagyságával, ami különösen alkalmassá teszi ezen mechanizmust arra, hogy anti-epileptikus gyógyszerfejlesztési célpont lehessen. Fontos ebből a szempontból, hogy a cserefolyamat érdemi alkotói, mint például a putrescin-GABA szintetikus útvonal vagy a GAT-3 fehérje kifejeződése önmagukban is felerősödnek epileptikus körülmények között. From a pharmacological point of view, it is also important to note that the widely used AEDs levetiracetam and clobazam have been demonstrated to increase GAT-3 expression in the hippocampus.
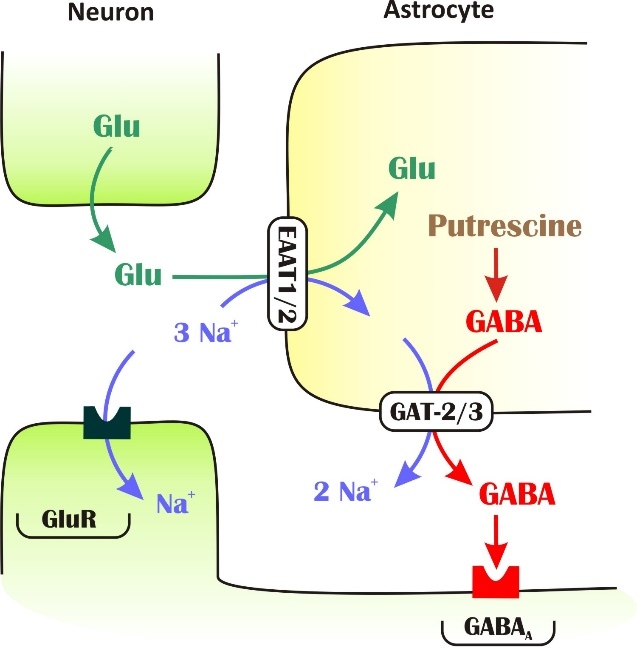 |
| A Glu/GABA cserefolyamat sematikus ábrázolása |
In addition to the GABA and Glu transporters, we also showed that blockade of intercellular gap junctional communication between astrocytes decreased the astrocytic synchronization and consequently inhibited or completely prevented the generation of recurrent SLEs. Therefore, the potential glial targets in AED development also includes another glial protein, the gap junction forming connexin43.
Hepatocyte-Kupffer cell cultures as advanced toxicity platforms
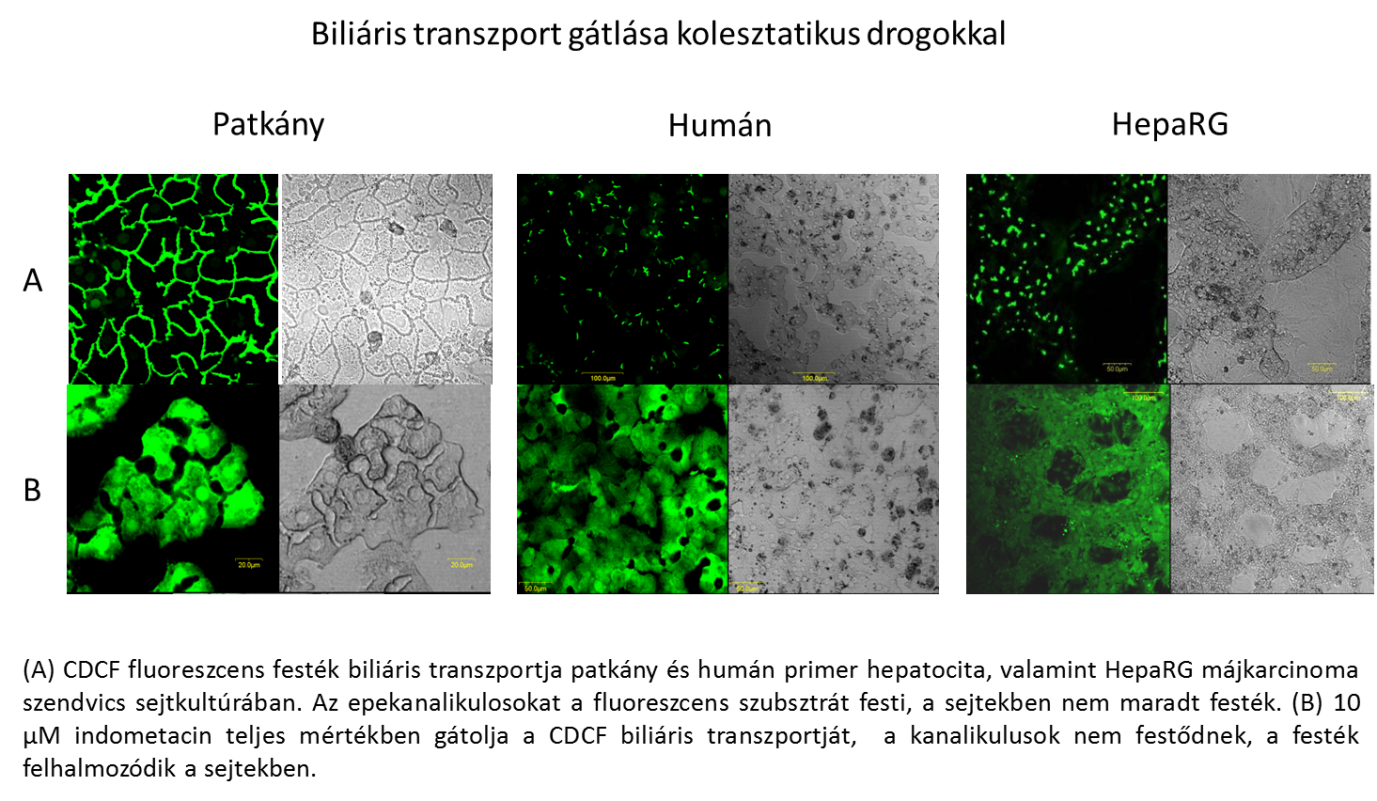
Munkacsoportunk további érdeklődési területe a máj uptake és efflux transzportereinek szerepe a gyógyszerindukált májkárosodás folyamatában, gyógyszerek és potenciális gyógyszermolekulák farmakokinetikai paramétereinek alakulásában, transzporter-gyógyszer interakciók vizsgálata. Tevékenységi körünkbe tartoznak gyógyszerek és potenciális gyógyszerek in vitro metabolizmusának felderítése, fázis I, fázis II metabolizáló enzimek és a máj transzporter proteinjeinek indukció és gátlás vizsgálatai. Jó eredményeket értünk el egy hepatocita-Kupffer sejt ko-kultúrán alapuló in vitro májmodell kidolgozásában, amelyet a nem parenchimális sejtek hepatoxikus folyamatokban játszott szerepének vizsgálatára fejlesztünk. A laboratórium citotoxicitás teszteket, Ca2+ homeosztázist, a fázis I, II enzimek, uptake és efflux transzporterek expresszióját, lokalizációját és funkcionális működését jellemző esszéket alkalmaz különféle fajokból (humán, rágcsáló, kutya) származó primer hepatocita szendvics kultúrában.
Új típusú hepatocita-Kupffer sejt kokultúra in vitro modell rendszereket fejlesztünk és alkalmazunk gyógyszerek és nanoanyagok toxikológiai szkrínelésére. A kutatóközpont más csoportjai részére rendszeresen végzünk toxikológiai vizsgálatokat.
A hepatotoxicitási vizsgálatokat szerves kémiai szintéziseink is támogatják. Fluoreszcensen jelzett epesavakat szintetizálunk, melyek az emésztésben és a lipid metabolizmusban betöltött szerepük feltárása miatt rendkívül fontosak. Használatukkal számos transzporter fehérje mint például az OATP (szerves anion transzporter fehérjék) és BSEP (epesav export pumpa fehérjék) működésének mechanizmusát tanulmányozhatjuk. Kutatásaink során epesavak NBD (4-nitrobenzo-2-oxa-1,3-diazol) konjugátumainak előállítását végezzük többlépéses szintézisek során.
 |
Műszerek, berendezések
- FEMTONICS 2D 2-foton mikroszkóp szimultán elektrofiziológiai detektálással, Ti-Sapphire lézer
- OLYMPUS FV300 konfokális pásztázó lézer mikroszkóp 458 nm, 488 nm, 514 nm, 543 nm, 633 nm-es lézerrel, infravörös kamera (CCDIR XC-EI50) és elektrofiziológiai detektálás
- Elektrofiziológiai és szimultán optikai képalkotó berendezés (OLYMPUS BX51WI mikroszkóp, Axopatch 200B and Multiclamp 700A erősítők, Digidata 1320 and Digidata 1322A konverterek & 5 MHz Micromax CCD kamera, NeuroPDA-III, WuTech H-469IV fotódióda mátrix
- Receptor- és transzporter farmakológiai laboratóriumok, mikrocentrifugák, szűrőberendezések
- Multi-mode microplate olvasók radioaktív és fluoreszecnscens detektálással
- Sejt- és szövettenyésztési laboratóriumok, hidegszoba
- HPLC, fluorimeter, ultracentrifuga, Western blot eszközök, mély-hűtők
- Hozzáférés a központ radioizotóp laboratóriumához, likvid szcintillációs számlálók
- Hozzáférés a központ állatházához
- Hozzáférés a Semmelweis Egyetem Humán Szövetbankjához
Együttműködések
- Semmelweis Egyetem
- Eötvös Loránd Tudományegyetem
- MTA, Szegedi Biológiai Kutatóközpont
- Szent István Egyetem
- Catholic University of Louvain,
- Charité, Berlin
- University of Copenhagen
- Biopredic International, France
- University of Rennes
- Richter Gedeon Gyógyszergyár
- Solvo Zrt.
- Toxi Coop Zrt.
Publikációk
Összesen: 47 publikáció 2013 – 2016 között
2016
Söveges, B.; Imre, T.; Szende, T.; Póti, Á. L.; Cserép, G. B.; Hegedűs, T.; Kele, P.; Németh, K., Systematic study of protein labeling by fluorogenic probes using cysteine targeting vinyl sulfone-cyclooctyne tags, Org. Biomol. Chem. 2016, doi: 10.1039/c6ob00810k.
Kozma, E.; Nikić, I.; Varga, B. R.; Aramburu, I. V.; Kang, J. H.; Fackler, O. T.; Lemke E. A.; Kele, P., Hydrophilic trans-Cyclooctenylated Non-Canonical Amino Acids for Fast Intracellular Protein Labeling, ChemBioChem 2016, doi: 10.1002/cbic.201600284.
Knorr, G.; Kozma, E.; Herner, A.; Lemke, E. A.; Kele, P., New, red-emitting tetrazine-phenoxazine fluorogenic labels for live-cell intracellular bioorthogonal labeling schemes, Chem. Eur. J. 2016, doi: 10.1002/chem.201600590.
Demeter, O.; Fodor, E. A.; Kállay, M.; Mező, G.; Németh, K.; Szabó, P. T.; Kele, P., A Double-Clicking Bis-Azide Fluorogenic Dye for Bioorthogonal Self-Labeling Peptide Tags, Chem. Eur. J. 2016, 22, 6382-6388.
Eördögh, Á.; Steinmeyer, J.; Peewasan, K.; Schepers, U.; Wagenknecht, H-A.; Kele, P., Polarity sensitive bioorthogonally applicable far-red emitting labels for postsynthetic nucleic acid labeling by copper-catalyzed and copper-free cycloaddition, Bioconjugate Chem. 2016, 27(2), 457-464.
2015
Cserép, G. B.; Herner, A.; Kele, P., Bioorthogonal fluorescent labels: a review on combined forces, Methods Appl. Fluoresc. 2015, 3(4), 042001.
Domonkos, C.; Zsila, F.; Fitos, I.; Visy, J.; Kassai, R.; Bálint, B.; Kotschy, A., Synthesis and serum protein binding of novel ring-substituted harmine derivatives, RSC Adv. 2015, 5, 53809-53818.
Cserép, G. B.; Demeter, O.; Bätzner, E.; Kállay, M.; Wagenknecht, H-A.; Kele, P., Synthesis and Evaluation of Nicotinic Acid Derived Tetrazines for Bioorthogonal Labeling, Synthesis 2015, 47, 2738-2744.
Castillo, G.; Pribransky, K.; Mező, G.; Kocsis, L.; Csámpai, A.; Németh, K.; Keresztes, Zs.; Hianik, T., Electrochemical and Photometric Detection of Plasmin by Specific Peptide Substrate, Electroanalysis 2015, 27(3), 789-798.
Huber, M. C.; Schreiber, A.; von Olshausen, P.; Varga, B. R.; Kretz, O.; Joch, B.; Barnert, S.; Schubert, R.; Eimer, S.; Kele, P.; Schiller, S. M., Designer amphiphilic proteins as building blocks for the intracellular formation of organelle-like compartments, Nat. Mater. 2015, 14, 125-132.
2014
Domonkos, C.; Fitos, I.; Visy, J.; Zsila, F., Role of the conformational flexibility of evodiamine in its binding to protein hosts: a comparative spectroscopic and molecular modeling evaluation with rutaecarpine, Phys. Chem. Chem. Phys. 2014, 16(41), 22632-22642.
Németh, K.; Domonkos, C.; Sarnyai, V.; Szemán, J.; Jicsinszky, L.; Szente, L.; Visy, J., Cationic permethylated 6-monoamino-6-monodeoxy-β-cyclodextrin as chiral selector of dansylated amino acids in capillary electrophoresis, J. Pharm. Biomed. Anal. 2014, 99, 16-21.
Stubinitzky, C.; Cserép, G. B.; Bätzner, E.; Kele, P.; Wagenknecht, H-A., 2’-Deoxyuridine Conjugated with a Reactive Monobenzocyclooctyne as a DNA Building Block for Copper-Free Click-type Postsynthetic Modification of DNA, Chem. Commun. 2014, 50, 11218-11221.
Herner, A.; Girona, G. E.; Nikić, I.; Kállay, M.; Lemke, E. A.; Kele, P., New Generation of Bioorthogonally Applicable Fluorogenic Dyes with Visible Excitations and Large Stokes Shifts, Bioconjugate Chem. 2014, 25(7), 1370-1374.
Cserép, G. B.; Baranyai, Zs.; Komáromy, D.; Horváti, K.; Bősze, Sz.; Kele, P., Fluorogenic tagging of peptides via Cys residues using thiol-specific vinyl sulfone affinity tags, Tetrahedron 2014, 70, 5961-5965.
Bobály, B.; Tóth, E.; Drahos, L.; Zsila, F.; Visy, J.; Fekete, J.; Vékey, K., Influence of acid-induced conformational variability on protein separation in reversed phase high performance liquid chromatography, J. Chromatogr. A 2014, 1325, 155-162.
2013
Cserép, G. B.; Herner, A.; Wolfbeis, O. S.; Kele, P., Tyrosine specific sequential labeling of proteins, Bioorg. Med. Chem. Lett. 2013, 23, 5776-5778.
Herner, A.; Nikić, I.; Kállay, M.; Lemke, E. A.; Kele, P., A new family of bioorthogonally applicable fluorogenic labels, Org. Biomol. Chem. 2013, 11, 3297-3306.
Cserép, G. B.; Enyedi, K. N.; Demeter, A.; Mező, G.; Kele, P., NIR Mega-Stokes Fluorophores for Bioorthogonal Labeling and Energy Transfer Systems – An Efficient Quencher for Daunomycin, Chem. Asian J. 2013, 8, 494-502.
Kele, P.; Li, X.; Duerkop, A., New luminescent ruthenium probes for detection of diacetyl, Microchem. J. 2013, 108, 156-160.
Oktatási tevékenység
- Modern biológia alapjai (ELTE-TTK, kötelezően választható kurzus) – őszi félév
- Bioortogonális kémia alapjai (ELTE-TTK, speciálkollégium) – tavaszi félév
- A molekuláris felismerés alapjai (ELTE-TTK, speciálkollégium) – tavaszi félév
Együttműködések
- Edward Lemke, EMBL, Heidelberg, Németország
- Hans-Achim Wagenknecht, Karlsruhe Institute of Technology, Karlsruhe, Németország
- Stefan Schiller, University of Freiburg, Freiburg, Németország
- Shixin Ye-Lehmann, ENS-Paris, Párizs, Franciaország
Vezető
Kele Péter

